Dysphotopsies
Les dysphotopsies regroupent les symptômes visuels indésirables qui surviennent généralement après une chirurgie de la cataracte avec pose d’un implant intraoculaire.
Ces symptômes comprennent la perception de croissants lumineux, brillants ou sombres, ou de halos, de stries ou de spicules à la périphérie du champ visuel, autour des sources lumineuses. Ils traduisent l’existence de trajets lumineux « inattendus » : réflexions multiples par les surfaces ou le bord de l’implant, ou encore des phénomènes de réfraction provoquant un éclairement asymétrique de la rétine périphérique.
Sommaire
À distinguer
Le terme de dysphotopsie est parfois employé pour désigner les halos lumineux induits par les implants multifocaux. Cette désignation est discutable : la perception de cercles lumineux autour des sources vives, la nuit, est attendue et directement liée au caractère multifocal de ces implants. Cette page concerne les dysphotopsies véritables, découlant de trajets lumineux parasites et imprévus.
Pourquoi les dysphotopsies surviennent-elles après chirurgie de la cataracte ?
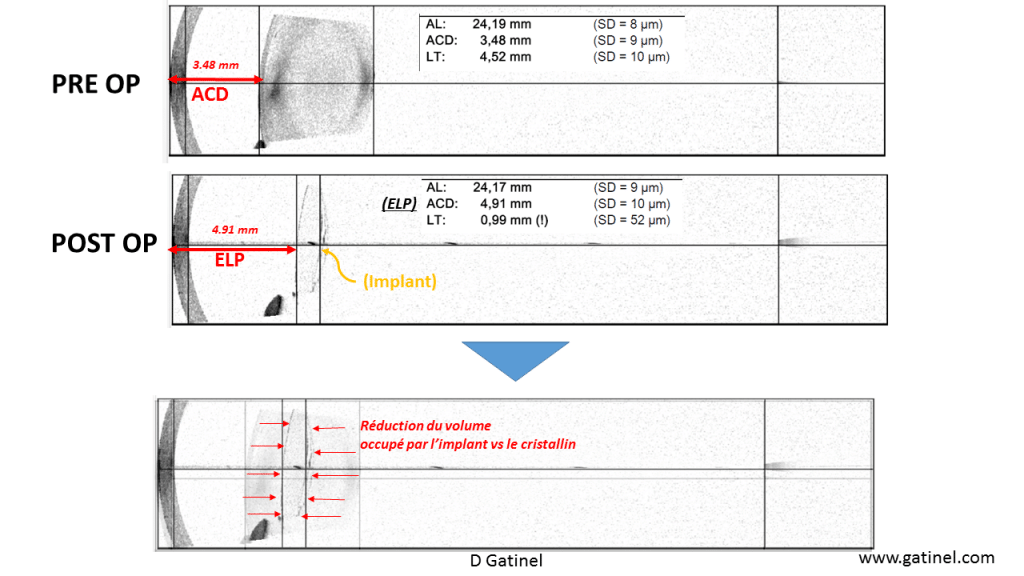
Les dysphotopsies sont la conséquence des modifications anatomiques et optiques engendrées par la chirurgie : le remplacement d’une lentille naturelle de fort volume et de faible indice (le cristallin) par une lentille artificielle de faible volume mais de fort indice (l’implant).
Ceci provoque l’apparition d’espaces libres de matériel réfractif, ouvrant la possibilité de trajets lumineux atypiques pour des rayons abordant l’œil à un angle particulier (rayons périphériques). L’arcade sourcilière limite l’incidence de ces rayons venant du haut, mais pas toujours quand ils viennent des régions latérales et temporales.

L’œil naturel est protégé
L’œil non opéré est relativement prémuni contre ce type de trajets lumineux car le cristallin occupe un volume important et « bouche » complètement l’orifice pupillaire. Il possède un indice de réfraction en gradient (du noyau vers le cortex), et ses surfaces courbes sont peu réfléchissantes, comme en atteste la difficulté à observer les images de Purkinje III et IV.
À l’inverse, l’implant présente un indice de réfraction constant et plus élevé, avec des surfaces optiques de plus faible rayon de courbure. Ces caractéristiques prédisposent aux réflexions indésirables. Un espace libre variable existe entre le bord de l’iris et la face antérieure de l’optique : s’il est large, certains rayons peuvent traverser directement vers la rétine sans être réfractés par l’implant.
Dysphotopsies positives
Définition
On parle de dysphotopsie positive quand l’œil opéré perçoit des lumières « vives » indésirables : arcs lumineux, halos, stries, scintillements, anneaux ou flashs de lumière.
Les dysphotopsies positives arciformes sont généralement rares et transitoires (atténuation en quelques semaines à mois). Jusqu’à 67 % des patients peuvent en percevoir immédiatement après la chirurgie, mais seuls environ 2 % conservent des symptômes persistants à un an.
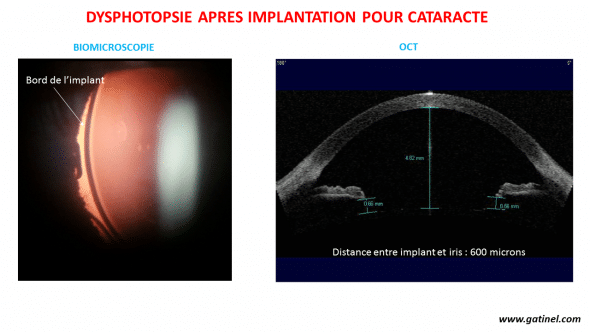
Elles se manifestent surtout lorsque la luminosité ambiante est faible et qu’une source lumineuse périphérique se situe dans le champ nasal ou temporaire. Elles tendent à s’atténuer avec la constriction pupillaire. Le mécanisme repose sur des réflexions au bord de l’implant, favorisées par les bords carrés et les matériaux à fort indice de réfraction.

Dysphotopsies négatives
Définition
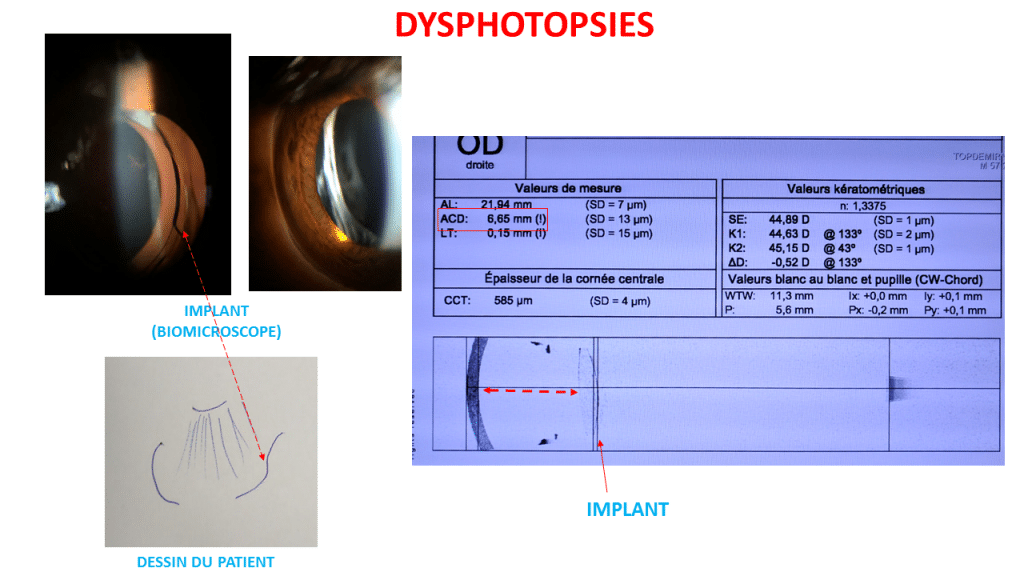
La dysphotopsie négative se caractérise par la perception d’un croissant sombre, toujours situé dans la portion temporale du champ visuel. Elle donne l’impression qu’une « œillère » limite la vision périphérique.
L’incidence atteint 15 à 26 % des patients en post-opératoire immédiat, mais les symptômes persistants (au-delà de 3 à 6 mois) ne concernent que 1 à 3 % des cas. La dysphotopsie négative reste une « énigme » pour la communauté ophtalmologique : aucune théorie unique n’explique pleinement le phénomène.
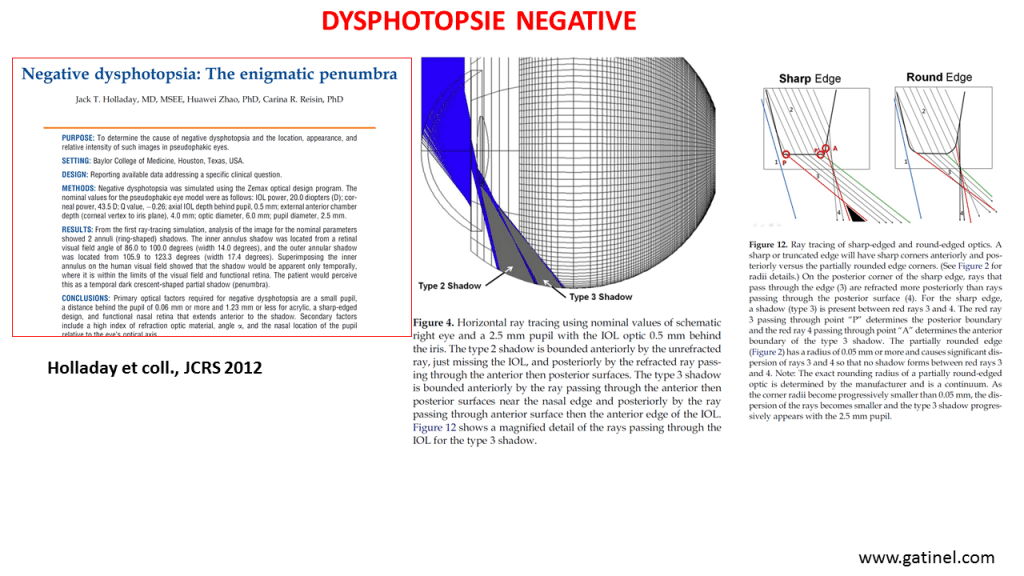
La théorie dominante, basée sur le ray tracing (Holladay 2012), est celle de l’« illumination gap » : certains rayons passent directement entre l’iris et l’implant sans être réfractés, tandis que d’autres sont réfractés par le bord de l’optique. Entre ces deux faisceaux apparaît une portion de rétine non ou peu illuminée, perçue comme un croissant sombre temporal.

Facteurs de risque
Dysphotopsie positive
- Bords d’implant carrés/anguleux
- Matériau à fort indice de réfraction
- Implants hydrophobes acryliques
- Forte réflectivité de surface
- Réflexions internes multiples
- Plis capsulaires
Dysphotopsie négative
- Petit diamètre pupillaire (photopique)
- Grand angle kappa
- Bords d’implant carrés
- Distance iris-implant prononcée
- Capsule antérieure nasale recouvrant l’IOL
- Implant de forte puissance dioptrique
- Implantation dans le sac (vs sulcus)
Prise en charge
La plupart des phénomènes visuels parasites disparaissent spontanément en quelques semaines à mois, grâce à deux mécanismes :
L’opacification progressive du sac capsulaire provoque une diffusion lumineuse accrue, atténuant les réfractions et réflexions anormales.
Le cortex visuel réduit progressivement l’importance de la perception subjective. Ce processus peut prendre 4 à 6 semaines, parfois jusqu’à un an.
Options thérapeutiques
Traitements conservateurs
- Réassurance du patient : expliquer le mécanisme et le caractère généralement transitoire
- Collyres myotiques (pilocarpine) pour dysphotopsie positive : la constriction pupillaire limite les réflexions du bord
- Collyres mydriatiques pour dysphotopsie négative : la dilatation augmente l’éclairement rétinien périphérique, « nivelant » les différences
- Attente de l’opacification capsulaire (quelques mois)
Options chirurgicales (symptômes persistants)
- Capsulotomie YAG nasale : ablation d’un secteur de capsule antérieure (résultats variables)
- Reverse optic capture : repositionnement de l’optique en avant du capsulorhexis, haptiques dans le sac
- Implant piggyback : ajout d’un implant en avant pour « boucher » le trajet des rayons parasites
- Échange d’implant : remplacement par un IOL de matériau différent (silicone, bords arrondis) → 85-90 % de succès pour les dysphotopsies positives
- Anneau anti-dysphotopsie (Masket ring) : dispositif spécifique
Prudence chirurgicale
L’échange d’implant est un geste délicat exposant à des complications (lésion de l’endothélium cornéen, rupture du sac capsulaire). Il est préférable d’attendre plusieurs mois et d’observer une opacification capsulaire spontanée avant d’envisager une réintervention.
Prévention
Le traitement des dysphotopsies est avant tout préventif. Malgré toutes les précautions, le risque n’est jamais nul après une chirurgie parfaitement menée.
Mesures préventives
- Orientation horizontale des haptiques : barrière naturelle contre les rayons périphériques latéraux
- Choix d’implants à bords arrondis ou texturés/givrés
- Diamètre d’optique ≥ 6 mm (vs 5.5 mm)
- Matériaux à faible indice de réfraction (silicone) pour les patients à risque
- Information préopératoire du patient sur ce risque transitoire
- Pour le 2e œil d’un patient ayant eu des dysphotopsies : changer de type d’implant
Évolutions technologiques
Les fabricants commencent à considérer la dysphotopsie comme un paramètre de conception, pas seulement une complication à gérer. Les implants en silicone (ex: Light Adjustable Lens) suscitent un regain d’intérêt pour leur faible indice de réfraction. De nouveaux designs (bords givrés, optiques spirales non diffractives) visent à réduire les réflexions parasites tout en maintenant la prévention de l’opacification capsulaire.
En résumé
Les dysphotopsies sont une cause fréquente d’insatisfaction après une chirurgie de la cataracte par ailleurs réussie. Elles sont liées aux propriétés optiques de l’implant (bords carrés, indice indice) et à sa position dans le segment antérieur. La majorité des cas s’améliorent spontanément en quelques semaines à quelques mois grâce à la neuroadaptation et à l’opacification capsulaire. Pour les cas persistants, des options chirurgicales existent, mais elles doivent être envisagées avec prudence.
Références
Articles fondamentaux
- Holladay JT, Zhao H, Reisin CR. Negative dysphotopsia: the enigmatic penumbra. J Cataract Refract Surg. 2012;38(7):1251-1265. [PDF]
- Davison JA. Positive and negative dysphotopsias in patients with acrylic intraocular lenses. J Cataract Refract Surg. 2000;26:1346-1355.
- Tester R, Pace NL, Samore M, Olson RJ. Dysphotopsia in phakic and pseudophakic patients: incidence and relation to intraocular lens type. J Cataract Refract Surg. 2000;26:810-816.
Revues et mises au point (2020-2025)
- Masket S, Fram NR. Pseudophakic Dysphotopsia: Review of Incidence, Cause, and Treatment of Positive and Negative Dysphotopsia. Ophthalmology. 2021;128(11):e195-e205.
- Milojković I, Petrović N. Dysphotopsias or Unwanted Visual Phenomena after Cataract Surgery. Medicina (Kaunas). 2023;59(1):37. [PMC]
- Jones C, Barnes J, Corbett G. Management of positive and negative dysphotopsia postcataract surgery – A literature review. Indian J Ophthalmol. 2025;73(7):S27-S34. [PMC]
- American Academy of Ophthalmology. Managing Dysphotopsias From Cataract Surgery. EyeNet Magazine. June 2023. [AAO]
Traitement chirurgical
- Masket S, Rupnick Z, Fram NR, et al. Surgical Management of Positive Dysphotopsia: US Perspective. J Cataract Refract Surg. 2020;46(11):1474-1479.
- Masket S, Fram NR, Cho A, Park I, Pham D. Surgical management of negative dysphotopsia. J Cataract Refract Surg. 2018;44(1):6-16.
- Folden DV. Neodymium:YAG laser anterior capsulectomy: Surgical option in the management of negative dysphotopsia. J Cataract Refract Surg. 2013;39:1110-1115.
Facteurs de risque et incidence
- Vashisht N, Vashisht T, Narang S, et al. Incidence and causes of negative dysphotopsia after uncomplicated cataract surgery – A randomized clinical trial. Indian J Ophthalmol. 2021;69(8):2048-2054. [PMC]
- Bournas P, Drazinos S, Kanellas D, et al. Dysphotopsia after cataract surgery: comparison of four different intraocular lenses. Ophthalmologica. 2007;221:378-383.
- Makhotkina NY, Berendschot TT, Nuijts RM. Objective evaluation of negative dysphotopsia with Goldmann kinetic perimetry. J Cataract Refract Surg. 2016;42:1626-1633.
Design d’implant et prévention
- Nishi O. Posterior capsule opacification. Part 1: Experimental investigations. J Cataract Refract Surg. 1999;25:106-117.
- Bonsemeyer MK, Thibos LN, Lane SS, et al. Optical quality after cataract surgery is affected by IOL material and decentration. J Cataract Refract Surg. 2020;46:1474-1480.
Pages connexes
Dernière mise à jour : février 2026
